Хімічні властивості лужноземельних металів. Застосування лужноземельних металів. Фізичні властивості лужноземельних металів
Розглянемо хімічні властивості лужноземельних металів. Визначимо особливості їх будови, отримання, знаходження в природі, застосування.
Положення ПС
Для початку визначимо розташування цих елементів у періодичній системі Менделєєва. Вони розташовуються у другій групі головної підгрупи. До них відносять кальцій, стронцій, радій, барій, магній, берилій. Всі вони на зовнішньому енергетичному рівні містять по два валентних електрона. У загальному вигляді берилій, магній і лужноземельні метали на зовнішньому рівні мають ns2 електронів. У хімічних сполуках вони виявляють ступінь окиснення 2. Під час взаємодії з іншими речовинами вони проявляють відновні властивості, віддаючи електрони зовнішнього енергетичного рівня.

Зміна властивостей
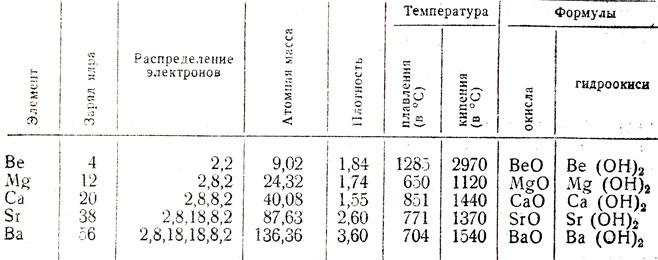
По мірі зростання ядра атома берилій, магній і лужноземельні метали посилюють свої металеві властивості, так як спостерігається зростання радіуса їх атомів. Розглянемо фізичні властивості лужноземельних металів. Берилій у звичайному стані є металом сірого кольору зі сталевим блиском. Він має щільну гексагональну кристалічну решітку. При контакті з киснем повітря, берилій відразу ж утворює оксидну плівку, в результаті чого знижується його хімічна активність, утворюється матовий наліт.
Фізичні властивості
Магній в якості простого речовини є білим металом, утворюючим на повітрі оксидне покриття. Він має гексагональну кристалічну решітку.
Фізичні властивості лужноземельних металів кальцію, барію, стронцію схожі. Вони являють собою метали з характерним сріблястим блиском, покриваються під впливом кисню повітря жовтуватою плівкою. У кальцію і стронцію кубічна гранецентрированная решітка, барій має об\’ємно-центрированную структуру.
Хімія лужноземельних металів грунтується на тому, що у них металевий характер зв\’язку. Саме тому вони відрізняються високою електричною і тепло провідністю. Температури їх плавлення і кипіння більше, ніж у лужних металів.

Способи отримання
Виробництво берилію в промислових обсягах здійснюється шляхом відновлення металу з фториду. Умовою протікання даної хімічної реакції є попереднє нагрівання.
Враховуючи, що лужноземельні метали в природі знаходяться у вигляді сполук, для одержання магнію, стронцію, кальцію проводять електроліз розплавів їх солей.

Хімічні властивості
Хімічні властивості лужноземельних металів пов\’язані з необхідністю попереднього усунення з їх поверхні шару оксидної плівки. Саме вона визначає інертність даних металів до води. Кальцій, барій, стронцій при розчиненні у воді утворюють гідроксиди, мають яскраво виражені основні властивості.
Хімічні властивості лужноземельних металів припускають їх взаємодія з киснем. Для барію продуктом взаємодії є пероксид, для всіх інших після реакції утворюються оксиди. У всіх представників даного класу оксиди проявляють основні властивості, тільки для оксиду берилію характерні амфотерні властивості.
Хімічні властивості лужноземельних металів проявляються і в реакцію з сіркою, галогенами, азотом. При реакціях з кислотами, спостерігається розчинення даних елементів. Враховуючи, що берилій відноситься до амфотерным елементів, він здатний вступати в хімічну взаємодію з розчинами лугів.

Якісні реакції
Основні формули лужноземельних металів, які розглядаються в курсі неорганічної хімії, пов\’язані з солями. Для виявлення представників даного класу в суміші з іншими елементами, можна використовувати якісне визначення. При внесенні солей лужноземельних металів в полум\’я спиртівки, спостерігається забарвлення полум\’я катіонами. Катіони стронцію дає темний червоний відтінок, катіон кальцію – оранжевий колір, а катіон барію зелений тон.
Для виявлення катіонів барію в якісному аналізі використовують сульфат-аніони. У результаті цієї реакції утворюється сульфат барію білого кольору, який розчиняється в мінеральних кислотах.
Радій є радіоактивним елементом, який у природі міститься в незначних кількостях. При взаємодії магнію з киснем, спостерігається сліпучий спалах. Даний процес деякий час застосовували під час фотографування в темних приміщеннях. Зараз на зміну магнієвим спалахів прийшли електричні системи. До сімейства лужноземельних металів відноситься берилій, який реагує з багатьма хімічними речовинами. Кальцій і магній аналогічно алюмінію, можуть відновлювати такі рідкісні метали, як титан, вольфрам, молібден, ніобій. Дані способи отримання металів називають кальциетермией і магниетермией.

Особливості застосування
Яке застосування лужноземельних металів? Кальцій і магній використовують для виготовлення легких сплавів і рідкісних металів.
Приміром, магній міститься в складі дюралюмінію, а кальцій – це компонент свинцевих сплавів, що використовуються для отримання оболонок кабелів та створення підшипників. Широко застосування лужноземельних металів у техніці у вигляді оксидів. Негашене вапно (оксид кальцію) і палена магнію (оксид магнію) потрібні для будівельної сфери.
При взаємодії з водою карбіду кальцію відбувається виділення значної кількості теплоти. Гашене вапно (гідроксид кальцію) застосовується для будівництва. Біла суспензія даної речовини (вапняне молоко) застосовують в цукровій промисловості для процесу очищення бурякового соку.
Солі металів другої групи
Солі магнію, берилію, лужноземельних металів можна отримати шляхом взаємодії з кислотами їх оксидів. Хлориди, фториди, іодіди даних елементів є білими кристалічними речовинами, в основному добре розчинними у воді. Серед сульфатів розчинністю мають тільки з\’єднання магнію і берилію. Спостерігається її зниження від солей берилію до сульфатів барію. Карбонати практично не розчиняються у воді або мають мінімальну розчинність.
Сульфіди лужноземельних елементів у незначних кількостях містяться у важких металах. Якщо направити на них освітлення, можна отримати різні кольори. Сульфіди включаються до складу світяться складів, іменованих фосфорами. Застосовують подібні фарби для створення світних циферблатів, дорожніх знаків.
Поширені сполуки рідкісноземельних металів
Карбонат кальцію є найпоширенішим на земній поверхні елементом. Він є складовою частиною таких сполук, як вапняк, мармур, крейда. Серед них основне застосування має вапняк. Цей мінерал незамінний в будівництві, вважається відмінним будівельним каменем. Крім того, з даного неорганічного з\’єднання отримують негашене і гашене вапно, скло, цемент.
Застосування вапняної щебінки сприяє зміцненню доріг, а завдяки порошку можна знизити кислотність грунту. Природний крейда являє собою раковини найдавніших тварин. Дане з\’єднання використовують для виготовлення гуми, паперу, створення шкільних крейди.
Мармур затребуваний у архітекторів, скульпторів. Саме з мармуру були створені багато унікальні творіння Мікеланджело. Частина станцій московського метро облицьована саме мармуровими плитками. Карбонат магнію у великих обсягах використовується при виготовленні цегли, цементу, скла. Він потрібен в металургійній промисловості для видалення пустої породи.
Сульфат кальцію, який міститься в природі у вигляді гіпсу (кристалогідрату сульфату кальцію), застосовується в будівельній галузі. У медицині дане з\’єднання застосовується для виготовлення зліпків, а також для створення гіпсових пов\’язок.
Алебастр (напівводний гіпс) при взаємодії з водою виділяє величезну кількість тепла. Це також застосовується в промисловості.
Англійська сіль (сульфат магнію) застосовується в медицині у вигляді проносного засобу. Дана речовина має гіркий смак, воно виявлено у морській воді.
«Баритовая каша» (сульфат барію) не розчиняється у воді. Саме тому цю сіль застосовують у рентгенодіагностиці. Сіль затримує рентгенівські промені, що дозволяє виявляти захворювання шлунково-кишкового тракту.
У складі фосфоритів (гірської породи) і апатитів є фосфат кальцію. Вони потрібні для отримання сполук кальцію: оксидів, гідроксидів.
Кальцій відіграє для живих організмів особливого значення. Саме цей метал необхідний для побудови кісткового скелета. Іони кальцію необхідні для регулювання роботи серця, підвищення згортання крові. Недолік його викликає порушення в роботі нервової системи, втрати згортання, втрату здатності рук нормально тримати різні предмети.
Для того щоб уникнути проблем зі здоров\’ям, кожні добу людина повинна споживати приблизно 1,5 грама кальцію. Основна проблема полягає в тому, що для того, щоб організм засвоював 0,06 грама кальцію, необхідно з\’їдати 1 грам жиру. Максимальна кількість цього металу міститься в салаті, петрушці, сирі, сирі.

Висновок
Всі представники другої групи головної підгрупи таблиці Менделєєва необхідні для життя і діяльності сучасної людини. Наприклад, магній є стимулятором обмінних процесів в організмі. Він повинен бути присутнім в нервової тканини, крові, кістках, печінці. Магній є активним учасником і фотосинтезу у рослин, так як він є складовою частиною хлорофілу. Кістки людини складають приблизно п\’яту частину від загальної ваги. Саме в них міститься кальцій і магній. Оксиди, солі лужноземельних металів знайшли різноманітне застосування в будівельній сфері, фармації і медицині.